Simultane Detektion: Multiplex-Tests
Die Multiplextechnologie ermöglicht die gleichzeitige Detektion mehrerer Pathogensequenzen in einer Probe und erhöht damit die Effizienz. Durch die gleichzeitige Analyse mehrerer Zielsequenzen werden Zeit und Probenmaterial effizienter genutzt und so die Kosten pro Test reduziert.
Die Durchführung von Multiplex-Tests kann komplex sein und erfordert sorgfältige Planung. Die LAMP-Technologie nutzt pro Nachweis sechs verschiedene Primer, was ein hohes Maß an Know-how bei der Gestaltung der Primer-Sets erfordert, um gegenseitige Interferenzen zu vermeiden. Unterschiede in der Effektivität der LAMP-Reaktionen können zur Dominanz des empfindlichsten Nachweises und zur Erhöhung des Risikos von Kreuzreaktivitäten führen.
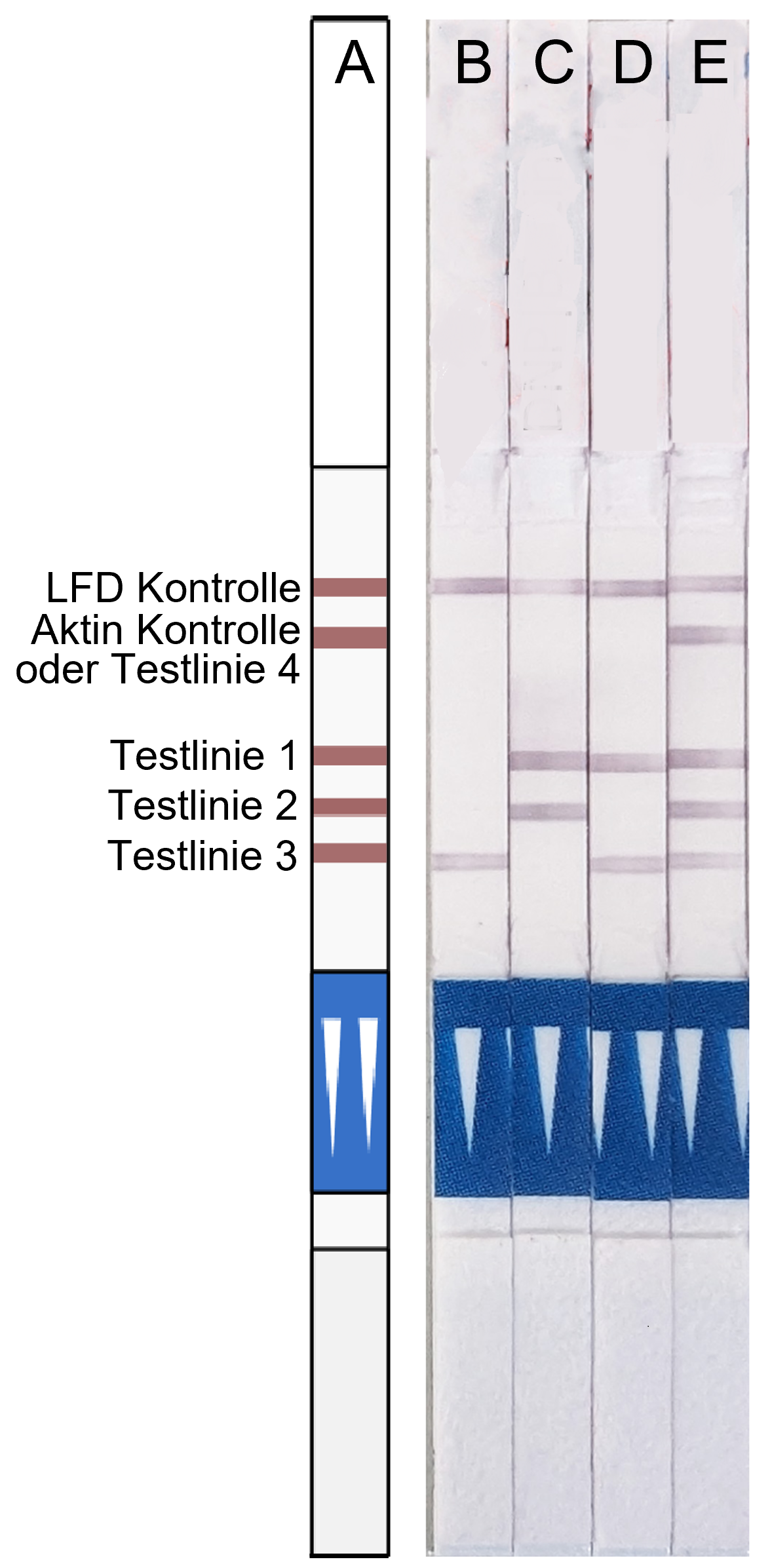
Zur Visualisierung der Ergebnisse nutzen wir Lateral Flow Dipsticks (LFD). Sie sind einfach zu handhaben und ermöglichen den spezifischen Nachweis von positiven Ergebnissen, was mit den meisten POC geeigneten LAMP-Nachweissystemen nicht möglich ist. Bei den LFD erfolgt dieser durch die spezifische Bindung der markierten Fragmente an den Teststreifen.
Die maximale Anzahl von Pathogenen in einem Multiplex-Assay wird nicht nur durch die Komplexität des Reaktionsaufbaus begrenzt, sondern auch durch die Anzahl der Testlinien auf den verfügbaren LFD. Bei der Entwicklung unseres Assays zum Nachweis von Kartoffelviren im Projekt »TRV2Go« standen lediglich LFDs mit maximal zwei adressierbaren Testlinien zur Verfügung, was maximal Duplex-Reaktionen erlaubte. Daher gaben wir im Projekt »2detect« die Entwicklung eines Teststreifens mit fünf Testlinien in Auftrag, um den gleichzeitigen Nachweis von bis zu vier verschiedenen markierten LAMP-Amplifikationsprodukten sowie einer Ziellinie für die interne LFD-Funktionskontrolle zu ermöglichen. In unserem Test verzichteten wir auf eine der Testlinien zugunsten einer weiteren Kontrolle, die mittels Amplifikation eines sogenannten Housekeeping Gens sicherstellt, das Probennahme, Setup der LAMP-Reaktion und Analyse der Ergebnisse durch den LFD fehlerfrei durchgeführt wurden, um falsch-positive sowie falsch negative Ergebnisse zu erkennen.
Wir nutzen diese Teststreifen erfolgreich für den Nachweis markierter Amplifikationsprodukte verschiedener humanpathogener respiratorischer Viren (RSV; Influenza A; Influenza B; SARS-CoV-2). In zukünftigen Projekten planen wir die Teststreifen auch für den differenzierten Nachweis weiterer Erreger beispielsweise von Nutztieren- oder Kulturpflanzen einzusetzen.
Fazit
Das neue LAMP-Testverfahren erfüllt die ASSURED-Kriterien und bietet bedeutende Vorteile im Bereich der Multiplex-Diagnostik. Durch die gleichzeitige Detektion mehrerer Pathogene aus einer Probe ermöglicht es eine effiziente und umfassende Analyse, die Zeit und Ressourcen spart. Die hohe Sensitivität des LAMP-Tests, insbesondere beim Nachweis von respiratorischen Viren, gewährleistet die zuverlässige Identifikation auch seltener Erreger. Dank seiner Benutzerfreundlichkeit und der Vermeidung komplexer Geräte ist der Einsatz in ressourcenarmen Gebieten und Notfallsituationen besonders attraktiv. Der neu entwickelte Teststreifen mit fünf Testlinien ermöglicht den simultanen Nachweis von bis zu 4 Erregern und trägt zur schnellen, präzisen und kosteneffizienten Diagnostik bei.
Die Fortschritte im Multiplexing positionieren unser LAMP-Testverfahren als zukunftsweisende Lösung in der Pathogendiagnostik, die die Anforderungen an Erschwinglichkeit, Sensitivität, Spezifität, Benutzerfreundlichkeit, Robustheit und Verfügbarkeit erfüllt.
 Fraunhofer-Institut für Molekularbiologie und Angewandte Oekologie IME
Fraunhofer-Institut für Molekularbiologie und Angewandte Oekologie IME