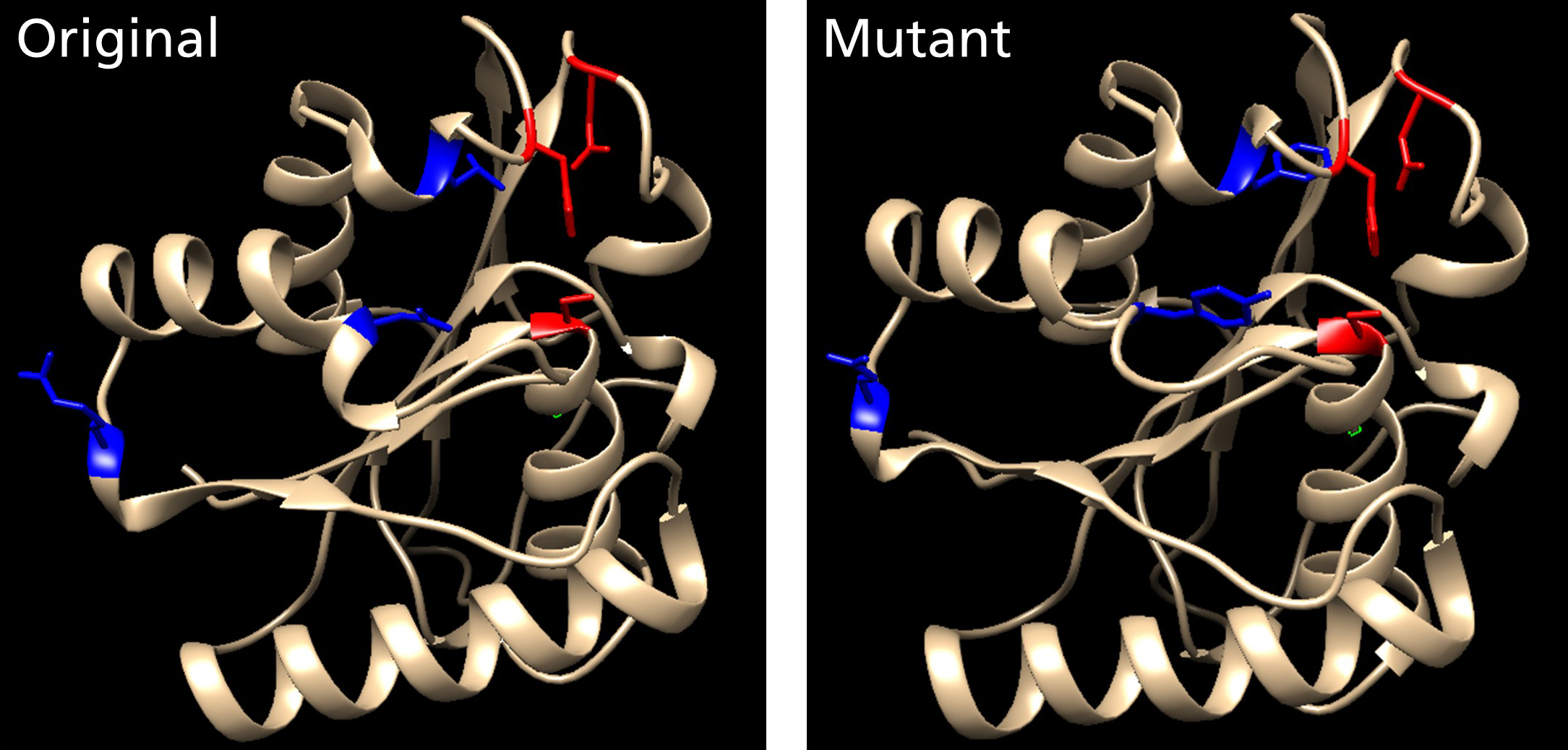
Enzyme können chemische Reaktionen spezifisch und schonend durchführen und sind deswegen ideal geeignet, die chemischen Katalysatoren in der Industrie zu ersetzen wobei Enzyme vorteilhafterweise eine hohe Spezifität mit einer niedrigen Toxizität und daher eine große Umweltfreundlichkeit zeigen. Natürlicherweise vorhandene Enzyme sind allerdings nicht immer für industrielle Prozesse geeignet. Eine Anpassung an den jeweiligen industriellen Prozess ist häufig notwendig und kann durch gerichtete Evolution erreicht werden. Dies ist ein Prozess durch den Mutationen in ein Protein-kodierendes Gen eingefügt werden und nachfolgend die Mutationsbibliothek in einem iterativen Ansatz nach Proteinen mit verbesserten Eigenschaften durchgemustert wird.
Der ausschlaggebende Teil bei der Entwicklung von neuartigen Enzymen ist immer die Durchmusterung und Auswahl von Varianten, da nur ein Test der sich auf die gewünschten neuen Eigenschaften stützt, gute Resultate bringt. Wir arbeiten dabei mit künstlichen Vesikeln, die durch Wasser in Öl–Emulsionen entstehen. Diese Vesikel agieren als Kleinstreaktionsgefäße und machen es möglich, dass wir mehr als 107 Enzymvarianten in weniger als einer Stunde durchmustern können. Jedes Vesikel enthält eine Enzymvariante und ein geeignetes Substrat, welches von dem Enzym in ein fluoreszierendes Produkt umgewandelt werden kann, falls die gewünschte Anpassung der Enzymaktivität erfolgreich war. Die fluoreszierenden, d.h. positiven Vesikel können mit Hilfe eines Durchflusszytometers oder in einem mikrofluidischem System von den negativen Ereignissen getrennt werden.
Am Fraunhofer IME wurden Enzymtests entwickelt und erfolgreiche Durchmusterungen von Enzymbibliotheken durchgeführt um besser angepasste Enzyme (z.B. Lipasen, Glucoseoxidase, Cellulasen und Peroxidasen) zu entwickeln.
 Fraunhofer-Institut für Molekularbiologie und Angewandte Oekologie IME
Fraunhofer-Institut für Molekularbiologie und Angewandte Oekologie IME